Syndrome hypoplasique du cœur gauche
Martina Feichter a étudié la biologie avec une spécialité pharmacie à Innsbruck et s'est également immergée dans le monde des plantes médicinales. De là, il n'était pas loin d'autres sujets médicaux qui la captivent encore à ce jour. Elle a suivi une formation de journaliste à l'Académie Axel Springer de Hambourg et travaille pour depuis 2007 - d'abord en tant que rédactrice et depuis 2012 en tant que rédactrice indépendante.
En savoir plus sur les experts Tout le contenu de est vérifié par des journalistes médicaux.
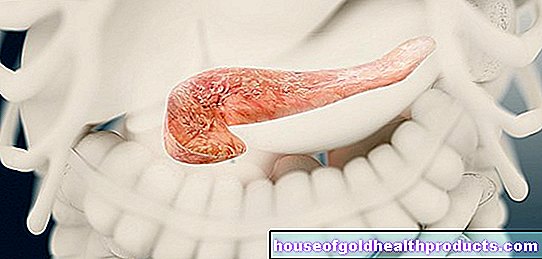
Le syndrome hypoplasique du cœur gauche (HLHS) est une anomalie cardiaque congénitale grave. La moitié gauche du cœur et l'artère principale sont sous-développées (= hypoplasique) ou présentent des défauts. Le résultat est une insuffisance cardiaque - le cœur ne peut pas pomper suffisamment de sang dans tout le corps. Si les bébés affectés ne sont pas traités rapidement, ils mourront. En savoir plus sur le syndrome du cœur gauche hypoplasique ici!
Codes CIM pour cette maladie : Les codes CIM sont des codes internationalement reconnus pour les diagnostics médicaux. On les retrouve, par exemple, dans les lettres des médecins ou sur les certificats d'incapacité de travail. Q23
Bref aperçu
- Qu'est-ce que le syndrome du cœur gauche hypoplasique (HLHS) ? Une grave malformation cardiaque congénitale dans laquelle le ventricule gauche et la partie de l'artère principale qui en dérive sont sous-développés. De plus, les valves cardiaques de la moitié gauche du cœur sont rétrécies ou fermées. Parfois, d'autres défauts accompagnent également le syndrome du cœur gauche hypoplasique.
- Causes : plusieurs changements (mutations) dans différents gènes
- Effets : Insuffisance cardiaque (insuffisance cardiaque), ce qui signifie que trop peu de sang est pompé dans le corps. Si elle n'est pas traitée, la HLHS est mortelle peu de temps après la naissance.
- Symptômes : par exemple respiration rapide, essoufflement, peau pâle et froide, pouls faible, peau et muqueuses bleuâtres
- Diagnostic : par échographie cardiaque ; un cathétérisme cardiaque est rarement nécessaire
- Traitement : les médicaments pour combler le temps jusqu'à la chirurgie en plusieurs étapes ou une transplantation cardiaque peuvent permettre une survie à plus long terme.
Qu'est-ce que le syndrome du cœur gauche hypoplasique (HLHS) ?
Le syndrome hypoplasique du cœur gauche (HLHS) est une anomalie cardiaque congénitale grave. Elle affecte principalement la moitié gauche du cœur et l'artère principale (aorte) qui en dérive. Le HLHS provoque une insuffisance cardiaque (insuffisance cardiaque), dont les conséquences conduisent à la mort sans traitement rapide.
Si une seule chambre cardiaque (ventricule) est complètement développée, comme dans le HLHS, les médecins parlent également d'un cœur à chambre unique ou d'un cœur univentriculaire.
Dans le détail, le syndrome hypoplasique du cœur gauche se caractérise par une combinaison des malformations suivantes :
Sous-développement du ventricule gauche : Le ventricule gauche est fortement sous-développé (hypoplasique), c'est-à-dire très petit. En conséquence, il n'est guère ou pas en mesure de remplir sa tâche, à savoir pomper le sang dans l'artère principale ramifiée (aorte) et donc plus loin dans le corps (organes abdominaux, bras, jambes, etc.).
Sous-développement de l'aorte ascendante : L'aorte ascendante (aorte « ascendante ») est la première section de l'artère principale (aorte) s'étendant du ventricule gauche. Elle n'est pas non plus correctement formée à HLHS.
Sous-développement de l'aorte isthmique : L'aorte isthmique est un goulot d'étranglement naturel de l'aorte à la transition entre l'arc aortique (deuxième section de l'aorte) et l'aorte descendante (aorte « descendante » ; troisième section de l'aorte).
Rétrécissement sévère (sténose) ou occlusion (atrésie) des valves cardiaques : La valve mitrale (entre l'oreillette gauche et le ventricule gauche) et la valve aortique (entre le ventricule gauche et l'aorte) sont affectées. Selon le type d'anomalie valvulaire cardiaque, il existe quatre sous-groupes de syndrome du cœur gauche hypoplasique, tels que MA/AoA (atrésie valvulaire mitrale et aortique) ou MS/AoA (sténose valvulaire mitrale et atrésie valvulaire aortique)
Parfois, le syndrome hypoplasique du cœur gauche s'accompagne d'autres malformations du cœur et des vaisseaux sanguins, comme une communication interventriculaire : Dans ce type de malformation cardiaque, le septum entre les deux cavités cardiaques n'est pas complètement fermé. Ou il y a aussi des malformations des artères coronaires. Certains enfants HLHS présentent également d'autres anomalies en dehors du cœur, comme un œsophage non continu ou un duodénum sous-développé (atrésie œsophagienne ou duodénale).
Le syndrome hypoplasique du cœur gauche survient dans jusqu'à dix pour cent des cas dans le cadre de syndromes génétiques tels que la trisomie 21 (syndrome de Down) ou le syndrome de Turner.
Syndrome hypoplasique du cœur gauche : fréquence
Le syndrome hypoplasique du cœur gauche est rare : il touche environ un à trois enfants sur 10 000 enfants nés vivants. Les garçons sont plus souvent touchés que les filles.
Le syndrome du cœur gauche hypoplasique représente environ un à deux pour cent de toutes les malformations cardiaques congénitales. Cependant, c'est l'une des causes les plus fréquentes d'insuffisance cardiaque (insuffisance cardiaque) chez les nouveau-nés. Le HLHS est également la cause la plus fréquente de décès d'origine cardiaque chez les bébés au cours de la première semaine de vie.
Que se passe-t-il au HLHS ?
Le syndrome hypoplasique du cœur gauche a des conséquences graves : le sous-développement et les malformations de la moitié gauche du cœur le rendent plus ou moins inopérable. La moitié droite du cœur doit assumer sa tâche : pomper le sang dans la circulation du corps. Cela n'est possible sans problème pour les enfants que peu de temps après la naissance, car ils ont des "courts-circuits" dans leur circulation sanguine :
Canal artériel et foramen ovale
Le canal artériel est une connexion vasculaire directe chez l'enfant à naître entre l'artère pulmonaire (provenant du ventricule droit et mène à la circulation pulmonaire) et l'aorte - plus précisément l'aorte "descendante" (aorte descendens), qui mène dans le corps circulation. Il est important pour la circulation sanguine du fœtus :
Les poumons de l'enfant n'ont pas à remplir et ne peuvent pas encore remplir leur fonction dans l'utérus (c'est-à-dire charger le sang en oxygène). Au lieu de cela, la mère fournit du sang oxygéné au fœtus. Il passe à travers le cordon ombilical dans la veine cave inférieure de l'enfant et dans l'oreillette droite. De là, il traverse le ventricule droit dans l'artère pulmonaire. Ici, seule une petite partie du sang est dirigée vers les poumons encore "fermés". Au lieu de cela, la majeure partie est transportée via le canal artériel directement dans l'artère principale (aorte) et donc plus loin dans la circulation corporelle.
Le foramen ovale peut également être utilisé pour contourner les poumons, qui ne commencent à fonctionner qu'après la naissance : il s'agit d'une petite ouverture naturelle dans le septum auriculaire du fœtus (à naître à partir de la 9e semaine de grossesse jusqu'à la naissance). Par cette ouverture, une partie du sang du cordon ombilical riche en oxygène peut s'écouler directement de l'oreillette droite vers l'oreillette gauche et ainsi être introduite dans la circulation du corps.
Après la naissance, les "courts-circuits" disparaissent
Dans les premiers jours après la naissance, le canal artériel se ferme et la circulation pulmonaire est élargie : le sang circulant du ventricule droit dans l'artère pulmonaire atteint maintenant complètement les poumons, où il est chargé en oxygène via l'air inhalé. Il retourne ensuite au cœur via les veines pulmonaires, du côté gauche du cœur, qu'il pompe ensuite dans la circulation corporelle - au moins chez les bébés sans HLHS.
Le foramen ovale se referme généralement tout seul peu après la naissance. Parfois, il reste partiellement ou complètement (foramen ovale ouvert).
HLHS : Après la naissance, les « courts-circuits » sont essentiels à la survie
Un canal artériel ouvert et une forme ovale ouverte assurent la survie des nouveau-nés atteints de HLHS : le sang enrichi en oxygène, qui provient du poumon maintenant dilaté et s'écoule dans l'oreillette gauche, peut atteindre l'oreillette droite via le foramen ovale ouvert. Là, il se mélange avec le sang désoxygéné du corps.
Le cœur continue de pomper ce « sang mélangé » dans les poumons via le ventricule droit. De là, une partie du sang s'écoule à travers le canal artériel encore ouvert dans la circulation du corps et maintient ainsi l'approvisionnement des organes et autres tissus.
La fermeture du canal artériel peu après la naissance a donc des conséquences dramatiques en cas d'hypoplasie du cœur gauche. Le ventricule gauche sous-développé peut difficilement ou pas du tout maintenir la circulation du corps.
À la suite de la fermeture du foramen ovale, le sang de l'oreillette gauche remonte également dans les poumons car il ne peut plus s'écouler dans l'oreillette droite. Cependant, le ventricule droit continue de pomper le sang vers les poumons. Le volume de sang dans les poumons augmente rapidement et la respiration se détériore sensiblement.
Syndrome hypoplasique du cœur gauche: symptômes
Le syndrome du cœur gauche hypoplasique se manifeste par des symptômes dès que le canal artériel commence à se fermer après la naissance (les enfants HLHS semblent donc généralement en bonne santé immédiatement après l'accouchement). Les bébés atteints développent rapidement des signes de choc cardiogénique (= choc d'origine cardiaque) :
- Respiration rapide
- Essoufflement
- pouls faible
- pâleur
- décoloration bleuâtre de la peau et des muqueuses (cyanose)
- basse température corporelle (hypothermie)
- acidose métabolique (acidose métabolique)
- Apathie (léthargie)
- diminution ou absence de miction (oligurie ou anurie) - donc presque pas de couches mouillées
En raison du sous-développement et des malformations de la moitié gauche du cœur et de l'aorte, trop peu de sang riche en oxygène se retrouve dans la circulation du corps. De plus, le flux sanguin vers les poumons continue d'augmenter par divers mécanismes. Cela met une pression énorme sur la respiration.
Si la situation circulatoire continue de se détériorer, il existe un risque d'infarctus cardiaque et cérébral (accident vasculaire cérébral dû à une diminution du débit sanguin). Des dommages à d'autres organes (tels que le foie, les intestins) peuvent également survenir en raison d'un apport sanguin insuffisant.
Si le canal artériel n'est pas réouvert immédiatement pour que la moitié droite du cœur puisse continuer à pomper le sang dans la circulation corporelle via ce "court-circuit", au moins pour le moment, le bébé mourra d'insuffisance cardiovasculaire !
Si un nouveau-né présente les symptômes décrits ci-dessus, un syndrome hypoplasique du cœur gauche est suspecté. Cela est particulièrement vrai si l'acidose métabolique du sang (acidose métabolique) s'aggrave après l'administration d'oxygène - un signe commun et caractéristique de HLHS. Parfois, les symptômes sont initialement interprétés à tort comme un « trouble de l'adaptation ». Si vous vous inquiétez pour votre bébé, il est préférable de reparler au pédiatre.
Syndrome hypoplasique du cœur gauche : diagnostic
Après chaque naissance, les pédiatres, entre autres, écoutent le cœur et mesurent la saturation en oxygène du sang (oxymétrie de pouls). Dans le HLHS, cependant, ces examens sont souvent normaux au début.
Un syndrome d'hypoplasie du cœur gauche peut être prouvé de manière fiable au moyen d'une échographie cardiaque (échocardiographie). Avec leur aide, le médecin peut évaluer l'importance du sous-développement et des malformations de la moitié gauche du cœur et de l'aorte et quel sous-type de HLHS est présent. Un examen à l'aide d'un cathéter cardiaque n'est que rarement nécessaire pour le diagnostic (en savoir plus sur cette procédure ici).
D'autres études fournissent des informations sur les effets et les dommages consécutifs possibles du syndrome hypoplasique du cœur gauche. Par exemple, différentes valeurs sanguines montrent à quel point le dysfonctionnement métabolique (hyperacidité) est prononcé. L'hypertrophie du muscle cardiaque (cardiomégalie), qui est généralement présente dans le syndrome du cœur gauche hypoplasique, peut être observée sur les radiographies pulmonaires (radiographie pulmonaire) - tout comme une hypertrophie des vaisseaux pulmonaires. La radiographie peut également montrer une accumulation de liquide dans les poumons (œdème pulmonaire).
Chez les enfants les plus touchés, le syndrome du cœur gauche hypoplasique est découvert dans l'utérus - lors de l'un des examens échographiques fournis pendant la grossesse ou d'un examen échographique cardiaque du fœtus. Les médecins initient alors un traitement pour le HLHS immédiatement après la naissance.
Comment traite-t-on le syndrome du cœur gauche hypoplasique?
Les médecins déplacent immédiatement les bébés atteints du syndrome du cœur gauche hypoplasique vers une unité de soins intensifs néonatals ou une unité de soins intensifs pour enfants atteints de maladie cardiaque. Là, vous pouvez non seulement le surveiller en continu, mais aussi le stabiliser jusqu'à ce qu'une opération soit possible.
Jusque-là, vous devez garder le canal artériel ouvert : Pour ce faire, le bébé reçoit une perfusion de prostaglandine E1 (PEG1). Ce principe actif peut empêcher la connexion en court-circuit entre l'artère pulmonaire et l'artère principale de se fermer ou peut complètement rouvrir le court-circuit.
Si les médecins ont déjà trouvé la malformation cardiaque dans l'utérus, le nouveau-né reçoit la perfusion de prostaglandine immédiatement après sa naissance.
De plus, les bébés atteints de HLHS sont stabilisés et traités au besoin. Les bébés gravement malades peuvent avoir besoin d'une ventilation mécanique pour assurer l'approvisionnement en oxygène du petit corps. Parfois, un bébé HLHS a également besoin de médicaments pour améliorer la fonction cardiovasculaire.
Procédure chirurgicale en trois étapes
Pour la survie continue des bébés atteints du syndrome du cœur gauche hypoplasique, les médecins recommandent généralement une intervention chirurgicale en plusieurs étapes : le cœur et les vaisseaux proches du cœur (comme l'aorte, l'artère pulmonaire) sont « remodelés » en trois interventions. En conséquence, le ventricule droit peut à l'avenir assumer la fonction du ventricule gauche sous-développé : il pompe le sang riche en oxygène des poumons vers la circulation corporelle.
Le sang "usé", pauvre en oxygène revenant des organes s'écoule directement dans les poumons via une dérivation sans aucune assistance de pompe du cœur. Après les trois interventions, les poumons et la circulation sanguine du corps fonctionnent pratiquement séparément les uns des autres avec une seule chambre cardiaque comme « moteur » (circulation de Fontan).
Le calendrier de la procédure chirurgicale en trois étapes:
- 1ère étape (procédure de Norwood / opération Norwood I, alternativement : thérapie hybride) : dans la première semaine de vie
- 2e stade (procédure bidirectionnelle de Glenn ou Hemi-Fontan, également appelée opération de Norwood II) : à l'âge de trois à six mois
- 3e stade (procédure de Fontan, également Norwood OP III) : à l'âge de 24 à 36 mois
Transplantation cardiaque
Dans les cas particulièrement graves, une transplantation cardiaque est parfois le meilleur choix de traitement pour le syndrome du cœur gauche hypoplasique qu'un remodelage cardiovasculaire en trois étapes. Jusqu'à ce qu'un cœur de donneur approprié soit disponible, les médecins continuent d'utiliser des perfusions de prostaglandines (et d'autres mesures nécessaires) pour maintenir le bébé en vie. Malheureusement, cela ne fonctionne pas toujours car l'offre de cœurs de donneurs est limitée. Environ 20 pour cent des bébés atteints de HLHS meurent en attendant une greffe.
Certains enfants avec un cœur à chambre unique développent une insuffisance cardiaque prononcée au fil du temps, même après une opération. Dans ces cas, une transplantation cardiaque est également souvent nécessaire.
Vivre avec HLHS
Un cœur gauche hypoplasique oblige certaines personnes à prendre des médicaments anticoagulants à long terme pour empêcher la formation de caillots sanguins. De nombreux enfants ont également besoin d'un ou plusieurs médicaments pour aider leur fonction cardiaque.
Certains enfants atteints de HLHS doivent prendre des antibiotiques avant un dentiste ou certaines opérations (par exemple sur les voies respiratoires). Il s'agit de prévenir l'inflammation bactérienne de la paroi interne du cœur (endocardite), qui peut survenir à la suite de telles interventions.
Les enfants qui ont subi une transplantation cardiaque d'un donneur doivent prendre des immunosuppresseurs à vie - des médicaments qui suppriment le système immunitaire afin qu'il ne rejette pas l'organe étranger. Comme effet secondaire, les personnes touchées sont plus sujettes aux infections. De plus, les immunosuppresseurs provoquent des modifications pathologiques des vaisseaux alimentant le cœur (artères coronaires) chez de nombreux enfants au cours des cinq premières années. Une nouvelle greffe cardiaque sera alors nécessaire.
HLHS : Complications
Certains enfants souffrent d'arythmie. Si le cœur bat trop lentement, un stimulateur cardiaque peut être nécessaire. Cependant, un cœur HLHS opéré peut également battre très rapidement. Dans ces cas, les médicaments peuvent également aider. Les médecins peuvent oblitérer une certaine partie du muscle cardiaque (ablation) afin que les impulsions électriques puissent se propager à nouveau régulièrement.
Une conséquence possible du HLHS - même après une opération réussie - est un affaiblissement du cœur à chambre unique. D'autre part, les médicaments peuvent agir sous des formes légères. Cependant, une transplantation cardiaque est parfois nécessaire.
Après une opération HLHS, les conditions de pression dans la circulation sanguine changent. Par exemple, la pression dans la veine cave est augmentée. En conséquence, les protéines s'échappent du sang vers les intestins, où elles provoquent des diarrhées (syndrome de perte de protéines / entéropathie). Les enfants atteints du syndrome du cœur gauche hypoplasique peuvent développer cette complication en vieillissant. En conséquence, la perte de protéines ne se produit chez certaines personnes qu'à l'adolescence.
Les poumons, plus précisément les bronches, peuvent également être touchés par ce type d'événement (bronchite fibroplastique). Les enfants atteints souffrent de fuites de liquide contenant des protéines et de la fibrine, de fortes quintes de toux et développent parfois de graves problèmes respiratoires. Les médecins tentent alors d'atténuer les symptômes par divers examens et mesures. Un régime riche en protéines peut être utile ou nécessaire si trop de protéines sont perdues.
Les troubles du développement sont souvent associés au syndrome du cœur gauche hypoplasique. Il est donc important que les enfants soient pris en charge en permanence par des pédiatres spécialisés et qu'ils bénéficient d'un accompagnement précoce ciblé.
Qualité de vie des enfants atteints de HLHS
La qualité de vie générale diffère d'un cas à l'autre. Certains enfants HLHS peuvent vivre presque normalement (jeu, jardin d'enfants, école, exercice léger). D'autres ont subi à plusieurs reprises de graves pertes de performances. Cependant, les performances physiques des personnes atteintes du syndrome du cœur gauche hypoplasique sont généralement généralement limitées par rapport aux personnes en bonne santé.
HLHS : espérance de vie
L'évolution et le pronostic du syndrome hypoplasique du cœur gauche dépendent en grande partie du type et de la gravité de la malformation cardiaque et de la durée du traitement. Le HLHS met définitivement la vie en danger : si un bébé naît avec le HLHS, sa survie immédiate dépend du maintien ou de la réouverture du canal artériel jusqu'à ce que l'enfant soit opéré (ou reçoive un nouveau cœur). Si elle n'est pas traitée, elle meurt en quelques jours à quelques semaines.
À quoi ressemblera l'espérance de vie et le pronostic à long terme dans un syndrome du cœur gauche hypoplasique opéré ne peut pas être prédit avec précision. Selon diverses études, 50 à 80 pour cent des enfants touchés sont encore en vie après cinq ans. Le taux de survie à 10 ans est estimé à environ 50 à 70 pour cent.
Le taux de survie à 5 ans après une transplantation cardiaque est similaire à celui après une intervention chirurgicale en plusieurs étapes.
La majorité des enfants atteints de HLHS aujourd'hui sont susceptibles d'atteindre l'âge adulte grâce à des thérapies améliorées. Cependant, si le syndrome du cœur gauche hypoplasique survient dans le cadre d'un syndrome génétique (tel que la trisomie 21, le syndrome de Turner) ou avec d'autres malformations, le pronostic s'aggrave.
Mots Clés: entretien grossesse médecine de voyage