Atrophie musculaire spinale
et Florian Tiefenböck, médecin Mis à jour leMaximilian Reindl a étudié la chimie et la biochimie au LMU de Munich et est membre de l'équipe éditoriale de depuis décembre 2020. Il se familiarisera pour vous avec les sujets médicaux, scientifiques et politiques de santé afin de les rendre compréhensibles et compréhensibles.
Plus de messages par Maximilian ReindlFlorian Tiefenböck a étudié la médecine humaine au LMU Munich. Il a rejoint en tant qu'étudiant en mars 2014 et a depuis soutenu l'équipe éditoriale avec des articles médicaux. Après avoir obtenu sa licence médicale et ses travaux pratiques en médecine interne à l'hôpital universitaire d'Augsbourg, il est membre permanent de l'équipe depuis décembre 2019 et veille, entre autres, à la qualité médicale des outils
Plus de messages par Florian Tiefenböck Tout le contenu de est vérifié par des journalistes médicaux.
L'amyotrophie spinale, ou SMA en abrégé, est une maladie rare dans laquelle certaines cellules nerveuses de la moelle épinière meurent. Les stimuli et impulsions du cerveau n'atteignent alors plus leur destination : les muscles. Cela provoque une fonte musculaire et une paralysie. Il existe différentes formes de SMA. La plus grave commence dans la petite enfance. De nouveaux traitements promettent une amélioration durable de la santé. En savoir plus sur les atrophies musculaires spinales ici.
Codes CIM pour cette maladie : Les codes CIM sont des codes internationalement reconnus pour les diagnostics médicaux. On les retrouve, par exemple, dans les lettres des médecins ou sur les certificats d'incapacité de travail. G12

Bref aperçu
- Qu'est-ce que l'amyotrophie spinale? Un groupe de maladies de faiblesse musculaire. Ils reposent sur la mort de certaines cellules nerveuses de la moelle épinière qui contrôlent les muscles (neurones moteurs). Par conséquent, les SMA font partie des maladies des motoneurones.
- Quelles formes existe-t-il ? Les atrophies musculaires spinales héréditaires sont principalement des SMA avec un certain défaut génétique sur le chromosome 5 (SMA associé à 5q). Les médecins distinguent quatre formes différentes : SMA type 1 - type 4. De plus, il existe des formes sporadiques dont l'hérédité n'est pas certaine.
- Fréquence : Maladie rare ; la SMA héréditaire touche environ un nouveau-né sur 7000.
- Symptômes : contractions musculaires, faiblesse musculaire progressive, atrophie musculaire, paralysie. Les gradients diffèrent selon la forme de l'AMS.
- Causes : Les amyotrophies spinales héréditaires de types 1 à 4 sont le résultat d'une anomalie génétique sur le chromosome 5, plus précisément sur le gène SMN1. En conséquence, le corps manque d'une protéine spéciale, la protéine SMN. Ce déficit endommage les motoneurones de la moelle épinière.
- Diagnostic : examen génétique pour la constitution génétique SMN modifiée, examens physiques, électroneurographie, électromyographie, tests sanguins (par exemple CK)
- Traitement : La thérapie de remplacement génique ou l'administration de médicaments de modulateurs d'épissage sont possibles. Accompagnement en physiothérapie, orthophonie, thérapie de la douleur et psychothérapie. Si nécessaire, chirurgie de la colonne vertébrale. Plan de traitement selon le type de SMA.
- Pronostic : Dans le cas de l'AMS proximale héréditaire, les nouvelles options thérapeutiques ont un effet causal et peuvent avoir un effet positif sur l'évolution de la maladie. Commencer le traitement tôt est crucial. Les traitements ne sont pas encore disponibles pour tous les patients. S'ils ne sont pas traités, les enfants atteints d'AS de type 1 meurent généralement au cours des deux premières années. Espérance de vie dans les types 3 et 4 peu ou pas réduite.
Qu'est-ce que l'amyotrophie spinale?
Dans l'amyotrophie spinale (SMA), certaines cellules nerveuses de la moelle épinière meurent. Ils contrôlent généralement les muscles, c'est pourquoi les experts appellent ces cellules nerveuses des motoneurones. En conséquence, les SMA appartiennent aux maladies dites des motoneurones.
Dans le cas des atrophies musculaires spinales, les neurones moteurs inférieurs (secondaires), qui sont directement connectés aux muscles avec leurs appendices, sont affectés. En raison des dommages, moins ou plus de signaux nerveux atteignent les muscles. Les muscles deviennent de plus en plus faibles et plus petits (atrophie musculaire / atrophie musculaire).
Les médecins distinguent les différentes formes d'amyotrophie spinale. Le groupe de loin le plus important est la SMA héréditaire, dans laquelle les muscles proches du tronc (proximaux) sont touchés. Ils sont basés sur un défaut génétique spécifique. Environ un nouveau-né sur 7 000 le développera.
L'amyotrophie spinale est une maladie rare dans l'ensemble. Néanmoins, c'est la deuxième maladie héréditaire autosomique récessive la plus fréquente et la cause la plus fréquente de décès chez les bébés ou les tout-petits en raison d'une anomalie génétique.
Quels types d'amyotrophie spinale existe-t-il?
Les médecins différencient les formes héréditaires (héréditaires) de la SMA des formes sporadiques. Une autre classification de l'amyotrophie spinale concerne principalement les groupes musculaires touchés en premier. Il y a
- SMA proximal : Avec environ 90 pour cent, ils forment le plus grand groupe SMA. Les symptômes commencent dans les muscles près du tronc, c'est-à-dire proximalement.
- SMA non proximal : Ici, les groupes musculaires plus éloignés, tels que les mains et les pieds, sont touchés en premier (SMA distal). Dans le cours ultérieur, ces SMA peuvent également se propager aux muscles près du milieu du corps.
- Formes particulières (ex : atrophie musculaire spinobulbaire de type Kennedy)
Atrophies musculaires spinales proximales
Les atrophies musculaires spinales proximales héréditaires sont pour la plupart des maladies basées sur un défaut génétique spécifique (SMA associé à 5q, défaut sur le chromosome 5). Ceux-ci sont à leur tour divisés en quatre formes différentes. La classification est basée sur le moment où les premiers symptômes apparaissent et sur l'évolution de la maladie.
Amyotrophie spinale de type 1 : Il s'agit de la forme la plus courante et la plus grave d'AMS. Elle est aussi appelée « maladie de Werdnig-Hoffmann » ou « SMA infantile aiguë ». La maladie débute généralement dans la petite enfance. La faiblesse musculaire affecte tout le corps - les médecins parlent aussi d'un « floppy infant syndrome » (de l'anglais floppy = flasque, infant = infant, child). La plupart des enfants non traités atteints d'AS de type 1 meurent avant l'âge de deux ans.
Amyotrophie spinale de type 2 : Cette forme d'AMS est également appelée « amyotrophie spinale intermédiaire » ou « SMA infantile chronique ». Les premiers symptômes apparaissent généralement avant l'âge de 18 mois. Les personnes touchées ont une espérance de vie parfois considérablement réduite.
Amyotrophie spinale de type 3 : Elle est également appelée « amyotrophie spinale juvénile » ou « maladie de Kugelberg-Welander ». Cette SMA commence généralement après l'âge de 18 mois et avant le début de l'âge adulte. La faiblesse musculaire est plus légère que dans le type 1 ou 2. Les personnes atteintes n'ont qu'une espérance de vie légèrement réduite.
Amyotrophie spinale de type 4 : Elle est similaire à l'AMS de type 3, mais n'apparaît qu'à l'âge adulte (généralement > 30 ans). Cependant, la faiblesse musculaire est moins prononcée et progresse plus lentement qu'avec l'AMS de type 3.
Les transitions entre les différentes versions sont fluides. Dans certains cas, cela rend difficile une démarcation claire. Certaines prédispositions génétiques jouent également un rôle important dans la gravité de la maladie en question.
Autres atrophies musculaires spinales
En plus de ces formes proximales, il existe d'autres formes d'amyotrophie spinale. Ceux-ci comprennent, par exemple, des atrophies musculaires spinales distales plus rares, également héréditaires. Avec eux, les symptômes commencent généralement dans les groupes musculaires les plus éloignés du corps.
L'héritage n'est pas garanti en cas de SMA sporadique. De plus, aucune accumulation familiale ne peut être déterminée. Dans la littérature, il s'agit de :
- Type Hirayama (SMA distale juvénile, maladie vers l'âge de 15 ans, affecte les muscles des bras, s'arrête généralement même sans traitement et peut même s'améliorer)
- Type Vulpian-Bernhard (également syndrome du « bras de fléau » avec apparition dans la ceinture scapulaire, généralement à partir de 40 ans)
- Type Duchenne-Aran (muscles de la main initialement touchés, s'étendant vers le tronc du corps, généralement après l'âge de 30 ans)
- Type péronier (syndrome "flail-leg", d'abord sur les muscles inférieurs de la jambe)
- Paralysie bulbaire progressive (troubles de la parole et de la déglutition, touche environ 20 % des patients atteints de sclérose latérale amyotrophique)
Certaines formes sporadiques de SMA (syndrome « fléau-bras-/-jambe », paralysie bulbaire progressive) sont comptées parmi les variantes de la sclérose latérale amyotrophique (SLA) dans les milieux spécialisés. Cet article traite principalement des atrophies musculaires spinales proximales héréditaires.
Atrophie musculaire spinobulbaire
L'atrophie musculaire spinobulbaire ou bulbospinale (type Kennedy, syndrome de Kennedy) est une maladie héréditaire. Il commence souvent au début de l'âge adulte moyen. Cette forme particulière de SMA est héritée de manière récessive liée à l'X et n'affecte donc que les hommes (puisque les hommes n'ont qu'un chromosome X, chez les femmes le deuxième chromosome X sain prédomine et compenserait le défaut).
La faiblesse musculaire des muscles proches du corps sur les jambes et les bras ou les épaules ainsi que les muscles de la langue et de la gorge est courante. En conséquence, les personnes concernées ont des difficultés à parler et à avaler, par exemple. Ils se plaignent également de tremblements, de crampes musculaires et de contractions musculaires. Les hommes affectés ont aussi souvent des testicules rabougris et sont stériles. De plus, les glandes mammaires grossissent (gynécomastie).
L'atrophie musculaire spinobulbaire est généralement lente. L'espérance de vie n'est guère limitée.
Comment reconnaître l'amyotrophie spinale?
L'amyotrophie spinale typique est une faiblesse musculaire progressive pouvant aller jusqu'à la paralysie (parésie) et des contractions musculaires. En raison des lésions nerveuses, les muscles ne reçoivent plus d'impulsions électriques, ce qui les fait rétrécir avec le temps (atrophie musculaire). Les signes et plaintes exacts dépendent de la forme respective. La section suivante examine les symptômes de l'AMS proximale héréditaire.
Symptômes de l'amyotrophie spinale infantile de type 1
Avec l'AMS de type 1, les symptômes apparaissent au cours des six premiers mois de la vie. Une faiblesse musculaire généralisée se produit - c'est-à-dire qui affecte tout le corps. De plus, la tension entre les muscles diminue. Les médecins parlent d'hypotonie.
Chez les nouveau-nés, cette faiblesse musculaire se manifeste d'abord par une posture typique des jambes, qui rappelle celle d'une grenouille couchée (posture des jambes de grenouille). Les jambes sont pliées, les genoux inclinés vers l'extérieur et les pieds inclinés vers l'intérieur. Même soulever ou tenir la tête par vous-même n'est généralement pas possible.
À un âge avancé, les enfants atteints d'AS de type 1 ne peuvent ni s'asseoir ni marcher seuls. De nombreux enfants sont également incapables de parler, car les muscles de la langue peuvent également être affectés.
Une autre caractéristique de l'amyotrophie spinale de type 1 est la forme du haut du corps : les muscles de la poitrine et du dos ne se développent pas correctement. Cela donne au haut du corps une forme en cloche (poitrine en cloche). En raison du faible développement des muscles de la poitrine et du dos, les personnes touchées adoptent une posture voûtée.
Souvent, il y a aussi une courbure croissante de la colonne vertébrale (scoliose). La posture voûtée vers l'avant et voûtée provoque d'autres problèmes respiratoires. Une respiration très rapide et superficielle (tachypnée) est caractéristique.
Symptômes de l'amyotrophie spinale intermédiaire de type 2
L'amyotrophie spinale de type 2 ne provoque généralement des symptômes qu'entre l'âge de sept et 18 mois. Les enfants atteints peuvent s'asseoir seuls, mais n'apprennent généralement pas à se tenir debout ni à marcher. La faiblesse musculaire progresse plus lentement que dans le type 1.
Avec l'AMS de type 2, des symptômes similaires à ceux de la forme infantile sévère, comme une déformation de la colonne vertébrale, apparaissent avec le temps. Les articulations se raidissent en raison du raccourcissement des muscles et des tendons (contractures). D'autres signes incluent des tremblements dans les mains et des contractions musculaires de la langue.
Symptômes de l'amyotrophie spinale juvénile de type 3
L'amyotrophie spinale de type 3 apparaît généralement après l'âge de 18 mois et avant l'âge de 18 ans. Les enfants atteints peuvent s'asseoir, se tenir debout et marcher de façon autonome. Cependant, la faiblesse musculaire, en particulier dans les muscles pelviens et des jambes, provoque une démarche dandinante.
Au fil des années, les performances diminuent : dans un premier temps, les personnes concernées trouvent les activités sportives ou la montée des escaliers difficiles, mais finalement il est également difficile de porter des sacs de courses, par exemple. Après de nombreuses années, l'amyotrophie spinale de type 3 rend la course et tout autre effort difficile voire impossible, même chez les personnes âgées.
Dans l'ensemble, cependant, les symptômes sont moins prononcés que dans les deux autres formes de maladie, le type 1 et le type 2. Pour beaucoup de personnes atteintes, la qualité de vie n'est guère altérée sur une longue période.
Symptômes de l'amyotrophie spinale adulte de type 4
Cette forme très rare de fonte musculaire progressive débute à l'âge adulte, souvent à partir de la troisième décennie de la vie. Les muscles des jambes et des hanches sont initialement touchés. Au fur et à mesure que la maladie progresse, la faiblesse musculaire se propage également aux épaules et aux bras.
La manifestation du tableau clinique est similaire à celle de l'AMS juvénile de type 3. Cependant, la faiblesse musculaire progressive est encore plus lente qu'avec l'AMS de type 3.
Qu'est-ce qui cause l'amyotrophie spinale?
Dans l'amyotrophie spinale, les deuxièmes motoneurones de la moelle épinière périssent. Ce sont des cellules nerveuses qui contrôlent les muscles avec leurs appendices. En raison des dommages causés à ces motoneurones hautement spécialisés, moins de signaux électriques atteignent les muscles que chez les personnes en bonne santé. Si les cellules musculaires sont moins sollicitées et donc moins stimulées, le corps les décompose avec le temps.
Défaut génétique
Dans la plupart des cas, l'amyotrophie spinale est une maladie héréditaire (SMA héréditaire). La cause des formes SMA proximales typiques est une information incorrecte dans la constitution génétique du patient. Le gène dit SMN1 sur le chromosome 5 n'est pas fonctionnel.
Le gène SMN1 porte l'information - c'est-à-dire le modèle - pour la molécule de protéine vitale appelée SMN. SMN signifie "Survival (of) Motor Neuron". Sans la molécule de protéine SMN, les motoneurones périssent avec le temps.
Il est vrai qu'il existe également un gène SMN2 apparenté dans le corps, qui est en principe capable de « compenser » l'information génétique SMN1 non fonctionnelle. Mais cela ne se produit généralement que dans une faible mesure. Cela signifie qu'une perte de fonction du gène SMN1 (si elle n'est pas traitée) ne peut généralement pas être complètement compensée par une copie intacte du gène SMN2.
Hérédité autosomique récessive et autosomique dominante
L'information génétique d'une personne est disponible en double. En conséquence, tout le monde possède deux copies du gène SMN1 - une de leur père et une de leur mère. Les atrophies musculaires spinales proximales de l'enfance sont généralement héritées comme un trait autosomique récessif.
Cela signifie que les deux variantes génétiques (allèles) des parents doivent être défectueuses pour que l'atrophie musculaire spinale se développe chez la progéniture. En cas d'hérédité récessive, les parents ne sont pas affectés car, en plus de celui sans fonction, ils possèdent également un gène SMN1 sain qui compense le défaut.
Environ une personne sur 45 est propriétaire de ce système pour SMA. Un couple dont les deux partenaires sont porteurs a 25 % de risque d'avoir un enfant atteint de la maladie.
Dans quelques cas à l'adolescence, les atrophies musculaires spinales à l'âge adulte en particulier suivent également une transmission autosomique dominante. Dans le cas de l'hérédité dominante, un gène défectueux s'affirme déjà - et les personnes affectées tombent malades. Cependant, il ne s'agit pas de l'anomalie génétique susmentionnée sur le chromosome 5. Ces SMA associées au 5q sont toujours héritées de manière autosomique récessive.
Héritage avec d'autres formes SMA
L'amyotrophie spinale non proximale peut également être héréditaire. La forme spinobulbaire spéciale (type Kennedy) est héritée de manière récessive via un chromosome sexuel, le chromosome X (cela affecte les variantes génétiques qui contiennent le plan des sites d'amarrage pour les hormones sexuelles mâles). Dans le cas des formes sporadiques, cependant, l'hérédité n'est pas garantie. On sait peu ici pourquoi exactement les deuxièmes motoneurones périssent.
Examens et diagnostic
Le diagnostic d'amyotrophie spinale est généralement posé par des pédiatres, des pédiatres spécialisés dans les maladies nerveuses (neuropédiatres) et des spécialistes des maladies du système nerveux (neurologues). Divers examens sont nécessaires pour une clarification plus précise. Dans le cas d'une SMA, les tests génétiques et les examens des nerfs et des muscles sont particulièrement importants.
Recueil des antécédents médicaux (anamnèse)
Avec chaque maladie, le médecin s'enquiert d'abord des symptômes qui se sont manifestés et de leur évolution jusqu'à présent. Chez les bébés et les tout-petits, les parents signalent des changements et des anomalies dans le comportement de leur enfant. Dans le cas des maladies héréditaires en particulier, les médecins se concentrent également sur les antécédents médicaux de la famille.
Examens physiques
Fondamentalement, un médecin détermine les anomalies du développement moteur en examinant physiquement l'enfant. Par exemple, il teste si les enfants peuvent indépendamment tenir la tête droite, s'asseoir ou bouger leurs bras ou leurs jambes de manière indépendante (selon leur âge).
Des tests d'effort complémentaires sont effectués chez les enfants plus âgés et les adultes suspects d'amyotrophie spinale. Le médecin vérifie combien de force la personne concernée peut rassembler et combien de temps elle peut la tenir. Il examine également l'endurance.
De plus, le médecin teste les réflexes, qui sont généralement affaiblis ou éteints, notamment en cas d'atrophie musculaire spinale prononcée. Pour ce faire, il tape différents tendons avec un marteau, par exemple sur le talon ou sous le genou, et vérifie la réaction.
Études génétiques
La méthode de détection la plus fiable pour l'amyotrophie spinale (héréditaire) est l'analyse génétique.Les médecins recherchent des preuves d'un gène SMN1 altéré (muté) et le nombre de copies SMN2 existantes.
La règle générale est de diagnostiquer et de traiter l'AMS (héréditaire) le plus tôt possible. Selon la forme et le traitement disponible, le développement moteur peut être influencé positivement avant que les motoneurones de la moelle épinière ne soient irréversiblement endommagés.
Enquêtes complémentaires à la SMA
Si une SMA est suspectée, les médecins mesurent souvent la vitesse de conduction des nerfs (électroneurographie) et l'activité musculaire (électromyographie). Si nécessaire, ils examinent également les muscles par échographie (myosonographie) ou imagerie par résonance magnétique (IRM).
De plus, les médecins organisent des analyses de sang. En cas d'amyotrophie spinale, certains paramètres peuvent être modifiés : par exemple, le niveau de créatine kinase (CK, une enzyme musculaire typique) est augmenté.
Traitement des atrophies musculaires spinales
Le traitement de l'amyotrophie spinale est complexe. Pendant longtemps, la thérapie causale n'a été possible pour aucune forme de SMA. Cependant, les progrès de la recherche médicale offrent aux médecins de nouvelles options de traitement pour aider fondamentalement les personnes atteintes de SMA proximale (anomalie du gène SMN sur le chromosome 5).
De plus, les médecins se concentrent sur l'atténuation des symptômes et le meilleur soutien possible aux personnes touchées (par exemple, physiothérapie, thérapie respiratoire, psychothérapie, éventuellement chirurgie).
Thérapie médicale
Les nouvelles approches thérapeutiques pour les patients chez qui la SMA est basée sur un défaut du gène SMN connu interviennent directement dans le matériel génétique lui-même ou dans le traitement en aval de l'information génétique.
L'objectif est de permettre au corps du patient de produire de manière autonome des quantités suffisantes de la protéine SMN, qui est cruciale pour les motoneurones.
Les options de traitement suivantes sont disponibles pour l'amyotrophie spinale :
- Modulateurs d'épissage (Nusinersen, Risdiplam) : Ces médicaments interviennent directement dans le traitement ultérieur des molécules d'ARN messager. Ils renforcent les processus qui délivrent une plus grande quantité de protéine SMN à partir du gène SMN2 intact.
- Thérapie de remplacement génique (Onasemnogene Abeparvovec) : Cette thérapie intervient directement dans le génome humain. La copie défectueuse du gène SMN1 est remplacée dans les cellules affectées par une construction génique fonctionnelle fournie de l'extérieur.
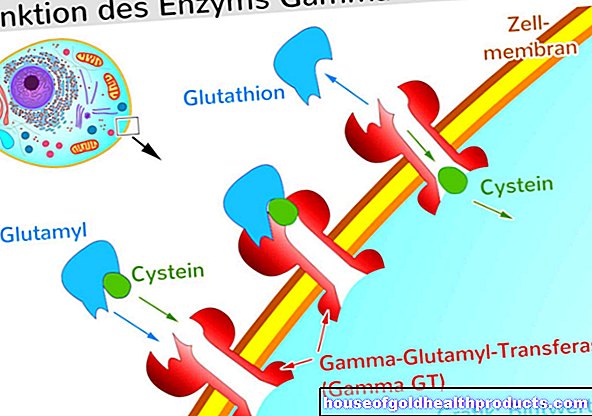
Modulateurs d'épissage
Dans le cas d'un défaut du gène SMN1, le corps peut alternativement produire la protéine SMN à partir du gène SMN2 apparenté. Le gène de remplacement SMN2 « saute dedans », mais cela ne suffit pas. La raison : les protéines de SMN2 sont généralement trop courtes et se décomposent rapidement.
Cela est dû au traitement de l'ARN messager SMN2 correspondant (ARNm SMN2). Il transmet les informations de construction du génome (ADN) aux sites de production de protéines (ribosomes).
Pour ce faire, le gène SMN2 dans le génome est d'abord lu. Un ARN messager SMN2 préliminaire est produit. Entre autres choses, il doit être traité davantage par ce que l'on appelle l'épissage. Ce n'est qu'alors que l'ARN messager mature apparaît. Des complexes cellulaires particuliers, les ribosomes, lisent alors l'ARN messager mature et produisent ainsi la protéine SMN2. Et c'est justement celle-ci qui est raccourcie et instable, se démonte rapidement et ne peut prendre en charge la fonction de SMN1.
Pour changer cela, les ingrédients actifs Nuusinersen et Risdiplam influencent le traitement ultérieur de l'ARN messager préliminaire. En conséquence, ces modulateurs d'épissage augmentent finalement la quantité de protéines SMN utilisables - et peuvent ainsi assurer un approvisionnement adéquat.
Nusinersen
Le médicament Nuusinersen est un soi-disant "oligonucléotide antisens" (ASO). Il a été approuvé par l'Agence européenne des médicaments en 2017. Les ASO sont des molécules d'ARN produites artificiellement et spécialement adaptées. Ils se lient spécifiquement et précisément à l'ARN messager SMN2. Cela les empêche d'être traités de manière incorrecte dans la cellule humaine.
Plus précisément : Nuusinersen empêche que des informations importantes (exon 7) soient coupées par erreur de l'ARN messager SMN2. La localisation de l'exon 7 amène le corps à fabriquer par la suite une protéine SMN plus fonctionnelle.
Nusinersen est administré par ce qu'on appelle une ponction lombaire. Cela signifie que le médicament est injecté dans le canal rachidien avec une seringue. Cette thérapie est répétée à intervalles réguliers de quelques mois. Au cours de la première année de traitement, les personnes atteintes reçoivent six, puis trois doses par an.
Les patients tolèrent généralement bien le médicament. Nusinersen conduit à des évolutions plus favorables de la maladie. Des études ont montré que la mobilité s'améliore chez de nombreux patients : dans de nombreux cas, il était possible de s'asseoir librement et de tourner le corps indépendamment. Les effets secondaires et les complications sont basés, entre autres, sur la ponction lombaire (par exemple maux de tête, infections des méninges).
Risdiplam
La Commission européenne a approuvé le Risdiplam comme troisième médicament contre la SMA associée au 5q (types 1-3 ou une à quatre copies du gène SMN2) en mars 2021. Risdiplam est pris quotidiennement sous forme de poudre dissoute. La dose exacte est calculée en fonction de l'âge et du poids corporel.
Contrairement à Nuusinersen, le Risdiplam n'est pas un "oligonucléotide antisens", mais une petite molécule. Cette molécule se lie à l'ARN messager des protéines SMN2 et les stabilise ainsi. En conséquence, des protéines SMN plus fonctionnelles sont créées.
Les effets secondaires courants du Risdiplam comprennent une gêne gastro-intestinale, des éruptions cutanées, de la fièvre et des infections des voies urinaires.
Thérapie de remplacement génique
Une autre approche du traitement de l'amyotrophie spinale proximale repose sur ce que l'on appelle la thérapie de remplacement génique. Le gène SMN1 défectueux - le point de départ de la SMA progressive - est "remplacé" par une nouvelle copie fonctionnelle du gène.
L'ingrédient actif Onasemnogene Abeparvovec (AVXS-101), qui fonctionne sur ce principe, a reçu une autorisation de mise sur le marché conditionnelle pour le traitement des tout-petits et des enfants de l'Agence européenne des médicaments (EMA) en mai 2020.
Le médicament peut être utilisé pour le SMA de type 1 selon les informations de l'EMA. Dans toutes les autres formes de SMA, les caractéristiques génétiques (nombre de copies SMN2) déterminent si la thérapie de remplacement génique est une option.
Avec Onasemnogene Abeparvovec, une copie fonctionnelle du gène humain SMN1 est introduite dans les cellules affectées de la moelle épinière et du tronc cérébral. Ceci est fait par certains virus qui servent de « bacs » pour le nouveau matériel génétique - les vecteurs viraux adéno-associés (vecteurs AAV).
Les constructions de gènes vecteurs sont administrées une fois sous forme de perfusion via la veine dans la circulation sanguine et de là sont distribuées dans tout le corps. En raison d'une barrière hémato-encéphalique pas encore complètement développée chez les jeunes enfants, ces vecteurs peuvent également pénétrer dans le tissu de la moelle épinière.
En liant préférentiellement ces vecteurs à des structures superficielles particulières des motoneurones, ils s'emparent préférentiellement du matériel génétique pour ensuite produire indépendamment la protéine SMN.
Le traitement peut améliorer les fonctions motrices et conduire à un succès développemental durable (par exemple, s'asseoir, ramper et marcher sans soutien).Au cours du traitement, les valeurs hépatiques peuvent parfois augmenter de manière significative, mais le nombre de plaquettes sanguines peut diminuer. La fièvre et les vomissements sont également fréquents. Pour réduire les effets secondaires, les patients reçoivent des corticostéroïdes (« cortisone ») pendant quelques semaines.
Un développement moteur adapté à l'âge n'est généralement possible que si la thérapie génique a commencé avant les symptômes. Le traitement a lieu dans des centres de traitement neuromusculaires spécialisés.
thérapie physique
La physiothérapie continue d'être un pilier important du traitement de la SMA.Toutes les formes de SMA ne peuvent pas être traitées avec les nouvelles approches thérapeutiques. La thérapie par l'exercice régulier est conçue pour maintenir les capacités physiques et ralentir la dégradation musculaire.
Le physiothérapeute déplace passivement les parties du corps déjà paralysées. Les séquences de mouvements actifs, à leur tour, sont entraînées pour soutenir la mobilité et la force des muscles. Des massages ou des traitements de chaleur et de froid peuvent également aider. Ceux-ci servent également à se détendre et, dans certaines circonstances, à ralentir la dégénérescence.
Orthophonie
Dans certains cas, l'AMS affecte les muscles de la parole et de la déglutition. Ensuite, un exercice d'orthophonie aide. Il encourage les enfants à apprendre à parler. Même chez les patients plus âgés, cela peut généralement ralentir une détérioration de la parole. Les orthophonistes entraînent également une déglutition correcte.
Les physiothérapeutes et les orthophonistes soutiennent les personnes concernées avec une thérapie respiratoire ciblée.
Traitement anti-douleur
La thérapie de la douleur joue un rôle important, en particulier dans les stades les plus avancés de la maladie. Les médecins utilisent des analgésiques pour réduire la souffrance des personnes touchées.
opération
Étant donné que l'amyotrophie spinale peut entraîner une courbure sévère de la colonne vertébrale (scoliose), les médecins envisagent parfois une intervention chirurgicale. Ce faisant, ils raidissent spécifiquement la colonne vertébrale.
Cela donne aux personnes concernées une (certaine) stabilité de torse supplémentaire, qui permet non seulement une posture plus droite, mais protège également les os et les articulations. Une chirurgie de la colonne vertébrale peut également aider contre les problèmes respiratoires progressifs.
Soins psychothérapeutiques
Les maladies neuromusculaires telles que l'amyotrophie spinale représentent un stress psychologique important.Les patients et leurs proches traitent le diagnostic lors de séances individuelles et de groupe dirigées par une psychothérapie et développent des stratégies pour mieux faire face à la maladie.
Les groupes d'entraide et les représentants des patients offrent également un soutien important. Ils informent, conseillent et soutiennent les personnes touchées et leurs proches pour faire face aux défis d'une maladie SMA.
Chances de guérison des atrophies musculaires spinales
En cas d'amyotrophie spinale, le pronostic dépend principalement de la forme respective. Plus les symptômes apparaissent tard, meilleur est le cours. De plus, plus les médecins diagnostiquent tôt l'amyotrophie spinale, plus tôt ils peuvent mettre en place des mesures de traitement adaptées, avant même que les motoneurones n'aient été irréversiblement endommagés.
Les nouvelles options de traitement via les modulateurs d'épissage et la thérapie de remplacement génique ont un grand potentiel dans le traitement de l'AMS proximale - en particulier lors du démarrage (très) précoce du traitement. Cependant, les données pour un pronostic fiable à long terme sont toujours en attente. Seules d'autres études et des observations étroites sur l'innocuité des médicaments peuvent fournir une certitude supplémentaire au cours des (mois et) prochaines années. Avec les nouveaux médicaments, un contrôle à long terme de la maladie ou même un remède sont au moins envisageables.
L'AMS de type 1 est généralement une maladie grave. Les enfants qui développent l'AMS de type 1 ont (non traités) une espérance de vie très limitée. La faiblesse musculaire qui augmente rapidement dans tout le corps affecte également la respiration. Les conséquences sont une pneumonie aiguë et même une insuffisance respiratoire. Les enfants atteints meurent au cours des premières années de vie.
Le pronostic est légèrement meilleur pour l'AMS de type 2. L'espérance de vie varie en fonction de la gravité exacte de la maladie : certains meurent dans l'enfance, mais la plupart atteignent l'âge adulte. Tôt ou tard - si désiré - la respiration doit être soutenue dans les formes les plus sévères. Les personnes touchées restent mobiles à l'aide d'un fauteuil roulant.
Avec l'AMS de type 3, le pronostic est nettement meilleur, surtout si les premiers symptômes apparaissent tardivement. Les performances se dégradent progressivement au cours de plusieurs années. Dans la vieillesse, un fauteuil roulant ou même des soins permanents peuvent être nécessaires. L'espérance de vie n'est guère limitée par l'amyotrophie spinale de type 3.
L'amyotrophie spinale adulte (type 4) est encore plus lente que le type 3. Les gens ont généralement une espérance de vie normale.
Mots Clés: la santé des hommes partenariat sexuel la prévention